


Segundo a Anvisa, os diretores também dispensaram a análise de impacto regulatório e consulta pública para o registro devido ao grau de urgência da vacina e gravidade da doença.
“A medida possibilitará acelerar a disponibilização à população brasileira de vacinas contra o novo coronavírus, desde que demonstradas qualidade, segurança e eficácia conforme os requerimentos técnicos e regulatórios vigentes”, informou a agência, em comunicado.
No procedimento de submissão contínua, os dados técnicos deverão ser encaminhados à Anvisa conforme forem gerados. Assim, as empresas interessadas no registro de vacinas não precisam ter em mãos todos os documentos reunidos para apresentá-los ao órgão regulador.
Submissão contínua
Esse procedimento será normatizado apenas para as vacinas contra covid-19 a serem registradas no país. Segundo a Anvisa, outras autoridades regulatórias de referência, como a dos Estados Unidos, da Europa, da Suíça e da China, já utilizam a submissão contínua em situações específicas.
A proposta da Anvisa prevê o atendimento a dois critérios para uso desse procedimento diferenciado. Um deles se refere à exigência de um dossiê de desenvolvimento clínico de medicamento referente à vacina proposta, protocolado na agência. Outro critério é que a pesquisa esteja em fase 3 de desenvolvimento clínico.
As vacinas que tiverem a análise iniciada pelo procedimento de submissão contínua poderão ser submetidas ao pedido de registro formal após a conclusão da análise do último aditamento protocolado.
Além disso, a empresa deve ter dados suficientes de qualidade, eficácia e segurança para o estabelecimento de uma relação positiva de benefício e risco da vacina, considerando a indicação terapêutica solicitada à Anvisa.
A instrução normativa publicada hoje regulamenta artigo da Resolução nº 55/2010 da Anvisa, que diz que a empresa solicitante do registro poderá procurar a Coordenação de Produtos Biológicos para discutir aspectos relacionados ao desenvolvimento do produto, antes da submissão da documentação de registro.
Com informações da Agência Brasil.
Ceará contabiliza 288.122 casos de coronavirus e tem 9.461 mortes pela doença
 |
| Foto FCO Fontenele |
O Ceará chegou a 288.122 casos confirmados e 9.461 mortes pela Covid-19 nesta quarta-feira, 18 de novembro. Os números da plataforma IntegraSUS, da Secretaria da Saúde do Ceará (Sesa), foram atualizados às 9h30min de hoje. Segundo o balanço, nenhuma pessoa morreu de Covid-19 nas últimas 24 horas.
Foram realizados até agora 1.093.546 exames. Há 41.697 casos em investigação.
Com informações do O Povo.
Pfizer anuncia que vacina contra o coronavirus é segura e atinge 95% de eficácia
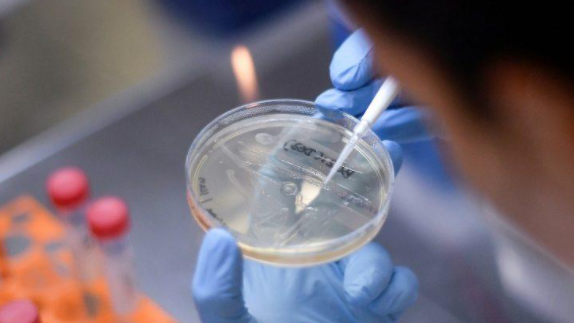 |
| Foto AFP |
A farmacêutica Pfizer anunciou nesta quarta-feira (18), que a sua vacina contra a Covid-19 é segura e tem 95% de eficácia. A conclusão foi extraída da terceira fase de testes da droga, elaborada em parceria com a empresa alemã BioNTech. Anteriormente, a farmacêutica já havia divulgado, baseando-se em resultados preliminares, que a vacina havia atingido 90% de eficácia
Segundo a Pfizer, a vacina previne as formas mais leves e graves da Covid-19. Até o momento, a droga também manteve praticamente a mesma taxa de eficácia para idosos, chegando a 94%.
O próximo passo será um pedido de autorização de emergência para FDA (Food and Drugs Administration), agência reguladora de medicamentos dos Estados Unidos. A Pfizer disse que isso será feito em "alguns dias".
Se as informações da Pfizer se confirmarem, o desenvolvimento da vacina quebrará todos os recordes de velocidade, pois é um processo que geralmente leva anos.
"Os resultados do estudo marcam um passo importante nessa jornada histórica de oito meses para apresentar uma vacina capaz de ajudar a acabar com essa pandemia devastadora", disse, em comunicado, o Dr. Albert Bourla, presidente-executivo da Pfizer.
Negociação com Brasil
Nesta última terça-feira (17), o presidente da Pfizer no Brasil, Carlos Murillo, disse que a empresa tem avançado nas negociações com o Ministério da Saúde e que, caso um acordo seja fechado, poderia disponibilizar vacinas já no primeiro trimestre de 2021.
A declaração ocorreu na saída de uma reunião na sede da pasta, em Brasília. "Estamos otimistas de que vamos a chegar a um bom entendimento", afirmou.
Segundo ele, as conversas com a pasta foram retomadas na última semana, após dados divulgados pela empresa apontarem que a vacina apresentou mais de 90% de eficácia na análise preliminar dos testes da fase três -a última etapa de estudos. Os resultados, no entanto, ainda são parciais e não correspondem à conclusão do ensaio clínico, em andamento também no Brasil. Ainda assim, os números levaram a empresa a retomar o diálogo com a pasta.
Questionado, Murillo não informou o número de doses em negociação, mas afirma que a oferta apresentada "permitiria vacinar alguns milhões de brasileiros no começo de 2021".
Segundo ele, caso haja conclusão dos estudos nos prazos previstos, a vacina pode estar disponível nos Estados Unidos e no Canadá em dezembro. No Brasil, o prazo mais otimista, diz, prevê possibilidade de oferta em janeiro.
Nenhum comentário:
Postar um comentário